- ارسال ها
- 113
- لایک ها
- 181
- امتیاز
- 0
پاسخ : انرژی یونش
سلام،بله ترتیب گفته شده درسته.
در واقع باید از یون یک بار مثبت هر کدوم از این اتم ها الکترونی بکنیم.
سدیم یک بار مثبت به دلیل اینکه تعداد تراز های الکترونی کمتری نسبت به دو اتم دیگه داره(شعاع کمتری داره،در نتیجه بار موثر هسته یا همون Z* بر الکترون های لایه ی ظرفیتش بیشتره) و همچنین به خاطر تقارن کامل آرایش الکترونیش به وضعیت پایداری از نظر سطح انرژی رسیده و مایل به از دست دادان الکترون نیست(به آرایش Ne رسیده)
رتبه ی بعدی به آلومینیوم یک بار مثبت تعلق داره که دارای سه تراز اکترونیه که همین باعث شده تا نیروی کمتری از سمت هسته به لایه ی ظرفیت اون وارد بشه و نسبت به سدیم انرژی یونش دوم کوچکتری داره. اما چون تعداد لایه های الکترونیش با منیزیم یک بار مثبت برابره،دیگه عامل تعداد لایه های دارای الکترون نمیتونه کمکی بکنه،اما چون زیر لایه ی 3s آلومینیوم یک بار مثبت،هنوز پره(تقارن نسبی خودشو حفظ کرده) نسبت به منیزیم پایداری بیشتری داره و سختتر میشه ازش الکترونی جدا کرد(هر چند میشه این عامل رو هم بیان کرد که چون آلومینیوم 13 پروتون در هسته ی خودش داره و این تعداد یک پروتون بیشتر از هسته ی منیزیمه،جاذبه ی قدرتمندتری بین الکترون های لایه ی آخر و هسته برقراره که باعث کوچکتر شدن شعاع اتمی آلومینیوم نسبت به منیزیوم میشه و به این دلیل سختر میشه از آلومینیوم الکترون جدا کرد. )
---- دو نوشته به هم متصل شده است ----
اگر توضیح کامل تری لازمه بیان کنید تا بنویسم.
سديم از همه بيشتره .
بعدش آلومينيوم.
بعدش منيزيم.
درسته ترتيبش؟
بعدش آلومينيوم.
بعدش منيزيم.
درسته ترتيبش؟
در واقع باید از یون یک بار مثبت هر کدوم از این اتم ها الکترونی بکنیم.
سدیم یک بار مثبت به دلیل اینکه تعداد تراز های الکترونی کمتری نسبت به دو اتم دیگه داره(شعاع کمتری داره،در نتیجه بار موثر هسته یا همون Z* بر الکترون های لایه ی ظرفیتش بیشتره) و همچنین به خاطر تقارن کامل آرایش الکترونیش به وضعیت پایداری از نظر سطح انرژی رسیده و مایل به از دست دادان الکترون نیست(به آرایش Ne رسیده)
رتبه ی بعدی به آلومینیوم یک بار مثبت تعلق داره که دارای سه تراز اکترونیه که همین باعث شده تا نیروی کمتری از سمت هسته به لایه ی ظرفیت اون وارد بشه و نسبت به سدیم انرژی یونش دوم کوچکتری داره. اما چون تعداد لایه های الکترونیش با منیزیم یک بار مثبت برابره،دیگه عامل تعداد لایه های دارای الکترون نمیتونه کمکی بکنه،اما چون زیر لایه ی 3s آلومینیوم یک بار مثبت،هنوز پره(تقارن نسبی خودشو حفظ کرده) نسبت به منیزیم پایداری بیشتری داره و سختتر میشه ازش الکترونی جدا کرد(هر چند میشه این عامل رو هم بیان کرد که چون آلومینیوم 13 پروتون در هسته ی خودش داره و این تعداد یک پروتون بیشتر از هسته ی منیزیمه،جاذبه ی قدرتمندتری بین الکترون های لایه ی آخر و هسته برقراره که باعث کوچکتر شدن شعاع اتمی آلومینیوم نسبت به منیزیوم میشه و به این دلیل سختر میشه از آلومینیوم الکترون جدا کرد. )
---- دو نوشته به هم متصل شده است ----
بله . ولی ممنون میشم کمی توضیح بدید دربارش .
- ارسال ها
- 2,196
- لایک ها
- 2,386
- امتیاز
- 0
پاسخ : انرژی یونش
آقاي 4everpersiangulf بسيار عالي و جامع توضيح دادن .
در مورد منيزيم و آلومينيوم كه بحثي نيست مي مونه سديم كه چون با جداكردن اولين الكترون يه لايه مياد بالاتر و ميشه گازنجيب دوره ي بالا ،
انرژي يونشش بيشتر از بقيه است.
ان شاء الله موفق باشيد.
بله . ولی ممنون میشم کمی توضیح بدید دربارش .
آقاي 4everpersiangulf بسيار عالي و جامع توضيح دادن .
در مورد منيزيم و آلومينيوم كه بحثي نيست مي مونه سديم كه چون با جداكردن اولين الكترون يه لايه مياد بالاتر و ميشه گازنجيب دوره ي بالا ،
انرژي يونشش بيشتر از بقيه است.
ان شاء الله موفق باشيد.
پاسخ : انرژی یونش
خیلی ممنون . ولی به نظر من منیزیم در دومین یونش خودش جهش داره و آیا این باعث نمیشه انرژی دومین یونشش از آلومینیم بیشتر بشه ؟
سلام،بله ترتیب گفته شده درسته.
در واقع باید از یون یک بار مثبت هر کدوم از این اتم ها الکترونی بکنیم.
سدیم یک بار مثبت به دلیل اینکه تعداد تراز های الکترونی کمتری نسبت به دو اتم دیگه داره(شعاع کمتری داره،در نتیجه بار موثر هسته یا همون Z* بر الکترون های لایه ی ظرفیتش بیشتره) و همچنین به خاطر تقارن کامل آرایش الکترونیش به وضعیت پایداری از نظر سطح انرژی رسیده و مایل به از دست دادان الکترون نیست(به آرایش Ne رسیده)
رتبه ی بعدی به آلومینیوم یک بار مثبت تعلق داره که دارای سه تراز اکترونیه که همین باعث شده تا نیروی کمتری از سمت هسته به لایه ی ظرفیت اون وارد بشه و نسبت به سدیم انرژی یونش دوم کوچکتری داره. اما چون تعداد لایه های الکترونیش با منیزیم یک بار مثبت برابره،دیگه عامل تعداد لایه های دارای الکترون نمیتونه کمکی بکنه،اما چون زیر لایه ی 3s آلومینیوم یک بار مثبت،هنوز پره(تقارن نسبی خودشو حفظ کرده) نسبت به منیزیم پایداری بیشتری داره و سختتر میشه ازش الکترونی جدا کرد(هر چند میشه این عامل رو هم بیان کرد که چون آلومینیوم 13 پروتون در هسته ی خودش داره و این تعداد یک پروتون بیشتر از هسته ی منیزیمه،جاذبه ی قدرتمندتری بین الکترون های لایه ی آخر و هسته برقراره که باعث کوچکتر شدن شعاع اتمی آلومینیوم نسبت به منیزیوم میشه و به این دلیل سختر میشه از آلومینیوم الکترون جدا کرد. )
---- دو نوشته به هم متصل شده است ----
اگر توضیح کامل تری لازمه بیان کنید تا بنویسم.
در واقع باید از یون یک بار مثبت هر کدوم از این اتم ها الکترونی بکنیم.
سدیم یک بار مثبت به دلیل اینکه تعداد تراز های الکترونی کمتری نسبت به دو اتم دیگه داره(شعاع کمتری داره،در نتیجه بار موثر هسته یا همون Z* بر الکترون های لایه ی ظرفیتش بیشتره) و همچنین به خاطر تقارن کامل آرایش الکترونیش به وضعیت پایداری از نظر سطح انرژی رسیده و مایل به از دست دادان الکترون نیست(به آرایش Ne رسیده)
رتبه ی بعدی به آلومینیوم یک بار مثبت تعلق داره که دارای سه تراز اکترونیه که همین باعث شده تا نیروی کمتری از سمت هسته به لایه ی ظرفیت اون وارد بشه و نسبت به سدیم انرژی یونش دوم کوچکتری داره. اما چون تعداد لایه های الکترونیش با منیزیم یک بار مثبت برابره،دیگه عامل تعداد لایه های دارای الکترون نمیتونه کمکی بکنه،اما چون زیر لایه ی 3s آلومینیوم یک بار مثبت،هنوز پره(تقارن نسبی خودشو حفظ کرده) نسبت به منیزیم پایداری بیشتری داره و سختتر میشه ازش الکترونی جدا کرد(هر چند میشه این عامل رو هم بیان کرد که چون آلومینیوم 13 پروتون در هسته ی خودش داره و این تعداد یک پروتون بیشتر از هسته ی منیزیمه،جاذبه ی قدرتمندتری بین الکترون های لایه ی آخر و هسته برقراره که باعث کوچکتر شدن شعاع اتمی آلومینیوم نسبت به منیزیوم میشه و به این دلیل سختر میشه از آلومینیوم الکترون جدا کرد. )
---- دو نوشته به هم متصل شده است ----
اگر توضیح کامل تری لازمه بیان کنید تا بنویسم.
- ارسال ها
- 113
- لایک ها
- 181
- امتیاز
- 0
پاسخ : انرژی یونش
نه ديگه !
وقتي ميخوايم سومين الكترون رو بكنيم ، اون موقع جهش بوجود مياد .
بله کاملا درسته.
ابتدا خوبه یه نیم نگاهی به آرایش نوشتاری منیزیوم و کاتیون های اون داشته باشیم.
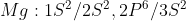



کندن اولین الکترون به مقداری انرژی نیاز داره که اونو با
 نمایش میدیم و بعد از کندن این الکترون اتم منیزیوم تبدیل به کاتیون
نمایش میدیم و بعد از کندن این الکترون اتم منیزیوم تبدیل به کاتیون
 میشه که میتونید آرایششو ملاحظه کنید.
میشه که میتونید آرایششو ملاحظه کنید.
کندن دومین الکترون هم به مقداری انرژی نیاز داره که مقدار اون کمی بیشتر از
 است و اونو با
است و اونو با
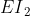 نمایش میدیم و پس از کندن این الکترون کاتیون
نمایش میدیم و پس از کندن این الکترون کاتیون
 تبدیل به کاتیون
تبدیل به کاتیون
 میشه که بازم میتونید آرایششو در بالا ملاحظه کنید.
میشه که بازم میتونید آرایششو در بالا ملاحظه کنید.
اما برای کندن الکترون سوم به انرژی خیلی زیاد تری نسبت به دو انرژی دیگه نیازه چرا که باید تقارن بوجود اومده بعد از کندن الکترون دوم رو از بین برد و از همه مهمتر از لایه ای نزدیکتر به هسته الکترون کند که به مراتب مشکل تر از کندن دو الکترون قبلی از لایه ی سومه.
پس اگر نموداری رسم کنیم تا این انرزی هارو با هم مقایسه کنیم ملاحظه میکنیم که بین مقدار های
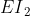 و
و
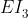 اختلاف زیادی وجود داره که به این اختلاف ناگهانی جهش بزرگ میگیم.(اگر در مفهوم جهش های بزرگ و کوچک ابهامی براتون وجود داره بیان کنید تا بسط بیشتری بدم.)
اختلاف زیادی وجود داره که به این اختلاف ناگهانی جهش بزرگ میگیم.(اگر در مفهوم جهش های بزرگ و کوچک ابهامی براتون وجود داره بیان کنید تا بسط بیشتری بدم.)
نه ديگه !
وقتي ميخوايم سومين الكترون رو بكنيم ، اون موقع جهش بوجود مياد .
ابتدا خوبه یه نیم نگاهی به آرایش نوشتاری منیزیوم و کاتیون های اون داشته باشیم.
کندن اولین الکترون به مقداری انرژی نیاز داره که اونو با
کندن دومین الکترون هم به مقداری انرژی نیاز داره که مقدار اون کمی بیشتر از
اما برای کندن الکترون سوم به انرژی خیلی زیاد تری نسبت به دو انرژی دیگه نیازه چرا که باید تقارن بوجود اومده بعد از کندن الکترون دوم رو از بین برد و از همه مهمتر از لایه ای نزدیکتر به هسته الکترون کند که به مراتب مشکل تر از کندن دو الکترون قبلی از لایه ی سومه.
پس اگر نموداری رسم کنیم تا این انرزی هارو با هم مقایسه کنیم ملاحظه میکنیم که بین مقدار های
