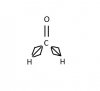
1- زاویه ی X-C-X را در COF2 , COCl2 ,COH2 مقایسه کنید
2-تعداد ایزومر های دی کلرو بنزن اگر پیوند های 2 گانه مکان مشخصی داشته باشند چقدر می باشند؟
3-کدام الکترولیت قوی تری هست ؟
الف: اسید فرمیک 0.02M ب:اسید استیک 0.02M
الف: اسید فرمیک 0.2M د:اسید استیک 0.2M
4- یه سوال خیلی ساده
عناصر گروه اول چند تان؟
2-تعداد ایزومر های دی کلرو بنزن اگر پیوند های 2 گانه مکان مشخصی داشته باشند چقدر می باشند؟
3-کدام الکترولیت قوی تری هست ؟
الف: اسید فرمیک 0.02M ب:اسید استیک 0.02M
الف: اسید فرمیک 0.2M د:اسید استیک 0.2M
4- یه سوال خیلی ساده
عناصر گروه اول چند تان؟