سلام. یه سوال داشتم. " pH محلول 10 -8 ( ده به توان منفی 8 ) مولار HCl در دمای 25 درجه سلسیوس برابر چند است؟" اگه بخوایم از فرمول H3O+] = n . M . a ] حلش کنیم جوابش میشه : 8 . ولی میدونم که اشتباهه! برای اینکه HCl اسیده و pH اون باید کمتر از 7 باشه. درضمن میدونم که باید خود-یونش آب رو هم در نظر بگیرم. اما نمیدونم اونو چه طوری دخالت بدم! اگه ممکنه راهنماییم کنید.( وقتی آدم سال سومه و پیش رو بخونه همین میشه دیگه! :x )
pH محلول
با سلام به شما دوست گرامی،
برای محاسبه pH یک محلول از رابطه زیر استفاده میشود:
در اینجا چون HCl اسید قوی است و به طور کامل تفکیک میشود، غلظت یون هیدرونیوم برابر همان غلظت اسید HCl است.
اگر غلظت را جایگزین کرده و مقدار لگاریتم را محاسبه کنی حاصل برابر 8 خواهد شد :roll:
این عدد عجیب به این خاطر به دست آمده است که شما از تفکیک مولکول های آب صرف نظر کرده اید. غلظت یون هیدرونیوم و هیدروکسید در آب خالص در دمای 25 درجه سلسیوس برابر 10 به توان 7- است که حدود 10 برابر غلظت اسید شما میباشد.
بنابراین در این غلظت بسیار کم باید غلظت یونهای اولیه آب را با اسید جمع کنی که حاصل برابر است با 6.95 = pH
موفق و پیروز باشی :twisted:
برای محاسبه pH یک محلول از رابطه زیر استفاده میشود:
کد
pH = -log[H+]اگر غلظت را جایگزین کرده و مقدار لگاریتم را محاسبه کنی حاصل برابر 8 خواهد شد :roll:
این عدد عجیب به این خاطر به دست آمده است که شما از تفکیک مولکول های آب صرف نظر کرده اید. غلظت یون هیدرونیوم و هیدروکسید در آب خالص در دمای 25 درجه سلسیوس برابر 10 به توان 7- است که حدود 10 برابر غلظت اسید شما میباشد.
بنابراین در این غلظت بسیار کم باید غلظت یونهای اولیه آب را با اسید جمع کنی که حاصل برابر است با 6.95 = pH
موفق و پیروز باشی :twisted:
nassim گفت
غلظت H3O+همون 10 به توان منفی 7 میمونه یا تغییر میکنه؟ به نظر خودم تغییر میکنه چون HCl توش حل شده. :x
ممکنه تغییر کند یا نکند! اما تا وقتی دما ثابت است نمیتوان تغییرات را محاسبه کرد و ما مجبوریم آن را بدون تغییر در نظر بگیریم.
البته با داشتن ثابت تعادل تفکیک HCl و آب در دمای معین میتوان مقدار دقیق غلظت را محاسبه نمود که خارج از اطلاعات داده شده در مساله است.
موفق باشی :twisted:
ما برای این کار از راه حل سیستماتیک استفاده می کنیم. این روش شامل نوشتن موازنه بار و موازنه جرم و تعادل های مربوطه. گونه های داخل Cl- و OH- و H+ هستند.همه OH- و مقداری H+ از یونش آب حاصل می شود.و بقیه +H از HCL بدست می آید.
موازنه بار : [-H+] = [Cl-] + [OH]
موازنه جرم: Cl-] = 10-8]
معادله تعادلی: [ - Kw= [H+] [OH
غلظت OH- را برابر x می گیریم پس:
H+] = 10-8+x]
حالا به حل معادله درجه 2 که از قرار دادن مقادیر بالا در ثابت تعادل آب مقدار X را بدست می آوریم.
X) ( 10-8 + X ) = 10-14)
که : X= 9.6 * 10-8 می شود.
پس : H+] = 1.06 * 10-7]
بنا براین PH = 6.98
که کاملا منطقی است و ثابت می کند که آب دارای خاصیت اسیدی است.
موازنه بار : [-H+] = [Cl-] + [OH]
موازنه جرم: Cl-] = 10-8]
معادله تعادلی: [ - Kw= [H+] [OH
غلظت OH- را برابر x می گیریم پس:
H+] = 10-8+x]
حالا به حل معادله درجه 2 که از قرار دادن مقادیر بالا در ثابت تعادل آب مقدار X را بدست می آوریم.
X) ( 10-8 + X ) = 10-14)
که : X= 9.6 * 10-8 می شود.
پس : H+] = 1.06 * 10-7]
بنا براین PH = 6.98
که کاملا منطقی است و ثابت می کند که آب دارای خاصیت اسیدی است.
- ارسال ها
- 1
- لایک ها
- 0
- امتیاز
- 0
پاسخ : pH محلول
با تشکر، من دانشجوی رشته دبیری شیمی ترم دوم هستم. این سوال رو استادمون دقیقا پرسید و من از پاسخ دادن بازموندم. تا اینجا متوجه شدم که باید تفکیک آب را در نظر داشت. مشکلم اینجاست که من دقیقا متوجه نشدم چگونه به عدد 6.95 رسیدید اگر پاسخ کامل بدید ممنون میشم.
با سلام به شما دوست گرامی،
برای محاسبه pH یک محلول از رابطه زیر استفاده میشود:
در اینجا چون HCl اسید قوی است و به طور کامل تفکیک میشود، غلظت یون هیدرونیوم برابر همان غلظت اسید HCl است.
اگر غلظت را جایگزین کرده و مقدار لگاریتم را محاسبه کنی حاصل برابر 8 خواهد شد :roll:
این عدد عجیب به این خاطر به دست آمده است که شما از تفکیک مولکول های آب صرف نظر کرده اید. غلظت یون هیدرونیوم و هیدروکسید در آب خالص در دمای 25 درجه سلسیوس برابر 10 به توان 7- است که حدود 10 برابر غلظت اسید شما میباشد.
بنابراین در این غلظت بسیار کم باید غلظت یونهای اولیه آب را با اسید جمع کنی که حاصل برابر است با 6.95 = pH
موفق و پیروز باشی :twisted:
برای محاسبه pH یک محلول از رابطه زیر استفاده میشود:
کد
pH = -log[H+]اگر غلظت را جایگزین کرده و مقدار لگاریتم را محاسبه کنی حاصل برابر 8 خواهد شد :roll:
این عدد عجیب به این خاطر به دست آمده است که شما از تفکیک مولکول های آب صرف نظر کرده اید. غلظت یون هیدرونیوم و هیدروکسید در آب خالص در دمای 25 درجه سلسیوس برابر 10 به توان 7- است که حدود 10 برابر غلظت اسید شما میباشد.
بنابراین در این غلظت بسیار کم باید غلظت یونهای اولیه آب را با اسید جمع کنی که حاصل برابر است با 6.95 = pH
موفق و پیروز باشی :twisted:
پاسخ : pH محلول
با سلام
پاسخ صحیح دقیقا 6.98 می باشد ... این دوستمون کاملا صحیح حل کردن ... اما آیا ما در دوران دبیرستان موازنه جرم و موازنه بار خونده ایم؟!
در مرحله دوم صرفا می بایست از اطلاعات غیر دانشگاهی استفاده کنیم!(بهتر بگم باید از دبیرستانی استفاده کنیم!)
به همین دلیل کافیه از
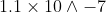 منفی لگاریتم بگیریم ... که جواب نهایی با 6.96 خواهد شد!
منفی لگاریتم بگیریم ... که جواب نهایی با 6.96 خواهد شد!
با سلام
پاسخ صحیح دقیقا 6.98 می باشد ... این دوستمون کاملا صحیح حل کردن ... اما آیا ما در دوران دبیرستان موازنه جرم و موازنه بار خونده ایم؟!
در مرحله دوم صرفا می بایست از اطلاعات غیر دانشگاهی استفاده کنیم!(بهتر بگم باید از دبیرستانی استفاده کنیم!)
به همین دلیل کافیه از
- ارسال ها
- 1
- لایک ها
- 0
- امتیاز
- 0
پاسخ : pH محلول
دقیقا من هم همین مشکل رو دارم.باید pH دقیق HClباغلظت 10به توان-9روبدست مساوردم.کسی هست واضح توضیح بده؟ممنون میشم
---- دو نوشته به هم متصل شده است ----
دقیقا من هم همین مشکل رو دارم.باید pH دقیق HClباغلظت 10به توان-9روبدست بیارم.کسی هست راهشو بم بگه؟ممنون میشم
---- دو نوشته به هم متصل شده است ----
من متوجه نشدم چیکارکردید؟
دقیقا من هم همین مشکل رو دارم.باید pH دقیق HClباغلظت 10به توان-9روبدست مساوردم.کسی هست واضح توضیح بده؟ممنون میشم
---- دو نوشته به هم متصل شده است ----
دقیقا من هم همین مشکل رو دارم.باید pH دقیق HClباغلظت 10به توان-9روبدست بیارم.کسی هست راهشو بم بگه؟ممنون میشم
---- دو نوشته به هم متصل شده است ----
من متوجه نشدم چیکارکردید؟
- ارسال ها
- 95
- لایک ها
- 54
- امتیاز
- 18
پاسخ : pH محلول
ببخشیدا ولی خیلی سادست چرا شماها اینقد سختش کردین
غلظت یون هیدرونیم کل برابر یون هیدروژن حاصل از خودیونش آب و یون هیدروژن حاصل از تفکیک هیدروکلریک اسیده.
چون غلظت هیدروکلریک اسید برابر 1*10[SUP]-8[/SUP] پس غلظت یون هیدروژن حاصل از تفکیک HCl برابر 10[SUP]-8[/SUP] *1 و همچنین غلظت یون هیدروژن حاصل از خودیونش آب هم که میدونیم [SUP]7-[/SUP]10 *1 . حالا اگه این دوتا رو باهم جمع بزنیم غلظت کل یون هیدروژن میشه [SUP]7-[/SUP]10*1.1 حالا منفی لگاریتم بگیریم میشه 6.96
دقیقا من هم همین مشکل رو دارم.باید pH دقیق HClباغلظت 10به توان-9روبدست مساوردم.کسی هست واضح توضیح بده؟ممنون میشم
---- دو نوشته به هم متصل شده است ----
دقیقا من هم همین مشکل رو دارم.باید pH دقیق HClباغلظت 10به توان-9روبدست بیارم.کسی هست راهشو بم بگه؟ممنون میشم
---- دو نوشته به هم متصل شده است ----
من متوجه نشدم چیکارکردید؟
---- دو نوشته به هم متصل شده است ----
دقیقا من هم همین مشکل رو دارم.باید pH دقیق HClباغلظت 10به توان-9روبدست بیارم.کسی هست راهشو بم بگه؟ممنون میشم
---- دو نوشته به هم متصل شده است ----
من متوجه نشدم چیکارکردید؟
ببخشیدا ولی خیلی سادست چرا شماها اینقد سختش کردین
غلظت یون هیدرونیم کل برابر یون هیدروژن حاصل از خودیونش آب و یون هیدروژن حاصل از تفکیک هیدروکلریک اسیده.
چون غلظت هیدروکلریک اسید برابر 1*10[SUP]-8[/SUP] پس غلظت یون هیدروژن حاصل از تفکیک HCl برابر 10[SUP]-8[/SUP] *1 و همچنین غلظت یون هیدروژن حاصل از خودیونش آب هم که میدونیم [SUP]7-[/SUP]10 *1 . حالا اگه این دوتا رو باهم جمع بزنیم غلظت کل یون هیدروژن میشه [SUP]7-[/SUP]10*1.1 حالا منفی لگاریتم بگیریم میشه 6.96
- ارسال ها
- 230
- لایک ها
- 350
- امتیاز
- 63
پاسخ : pH محلول
ببینین...
مگه تعادل آب نیست؟ مگه طبق واکنش هاش مثبت بدست اومده از آب با oh منفی آب برابر نیست؟ اینارو بگیریم برابر x
مگه ۱۰ به توان منفی9 تا هاش مثبت از اسید نداریم؟
خب ثابت تعادل تفکیک آب ۱۰ به توان منفی۱۴ ست دیگه....
پس ضرب غلظت هاش مثبت و oh منفی توی دمای اتاق همیشه برابر ۱۰ به توان منفی ۱۴ ست...
غلظت هاش مثبت = x+ ۱۰^-9
غلظت oh منفی = x
ضرب این دوتا بالایی ها میشه ۱۰ به توان منفی ۱۴
x میشه ۹.۹۵۰۱۲۴۵ ضربدر ۱۰ به توان منفی ۸
هاش مثبت هم میشه ۱.۰۰۵۰۱۲۵ ضربدر ۱۰ به توان منفی ۷
منفی لگاریتمش میشه۶.۹۹۷۸
دقیقا من هم همین مشکل رو دارم.باید pH دقیق HClباغلظت 10به توان-9روبدست مساوردم.کسی هست واضح توضیح بده؟ممنون میشم
---- دو نوشته به هم متصل شده است ----
دقیقا من هم همین مشکل رو دارم.باید pH دقیق HClباغلظت 10به توان-9روبدست بیارم.کسی هست راهشو بم بگه؟ممنون میشم
---- دو نوشته به هم متصل شده است ----
من متوجه نشدم چیکارکردید؟
---- دو نوشته به هم متصل شده است ----
دقیقا من هم همین مشکل رو دارم.باید pH دقیق HClباغلظت 10به توان-9روبدست بیارم.کسی هست راهشو بم بگه؟ممنون میشم
---- دو نوشته به هم متصل شده است ----
من متوجه نشدم چیکارکردید؟
مگه تعادل آب نیست؟ مگه طبق واکنش هاش مثبت بدست اومده از آب با oh منفی آب برابر نیست؟ اینارو بگیریم برابر x
مگه ۱۰ به توان منفی9 تا هاش مثبت از اسید نداریم؟
خب ثابت تعادل تفکیک آب ۱۰ به توان منفی۱۴ ست دیگه....
پس ضرب غلظت هاش مثبت و oh منفی توی دمای اتاق همیشه برابر ۱۰ به توان منفی ۱۴ ست...
غلظت هاش مثبت = x+ ۱۰^-9
غلظت oh منفی = x
ضرب این دوتا بالایی ها میشه ۱۰ به توان منفی ۱۴
x میشه ۹.۹۵۰۱۲۴۵ ضربدر ۱۰ به توان منفی ۸
هاش مثبت هم میشه ۱.۰۰۵۰۱۲۵ ضربدر ۱۰ به توان منفی ۷
منفی لگاریتمش میشه۶.۹۹۷۸
سلام دوستان یه سوال داشتم ممنون میشم اگه بگید چجوری باید حلش کنم.
مقدار [+H] و [_OH] را در محلول 0/02 مولار از HCL محاسبه کنید.[/QUO
غلظت اسید قوی که همون غلظت یون هیدرونیوم هست ، غلظت یون هیدروکسید هم که با ۱۰ به توان منفی چهار بدست میاد
مقدار [+H] و [_OH] را در محلول 0/02 مولار از HCL محاسبه کنید.[/QUO
سلام دوستان یه سوال داشتم ممنون میشم اگه بگید چجوری باید حلش کنم.
مقدار [+H] و [_OH] را در محلول 0/02 مولار از HCL محاسبه کنید.
مقدار [+H] و [_OH] را در محلول 0/02 مولار از HCL محاسبه کنید.
