.> ماراتون شیمی تجزیه! <.
پاسخ : .> ماراتون شیمی تجزیه! <.
راستش من فک کردم پی کا=1.92 که نوشتید، مربوط میشه به قسمت دوم سوال و به قسمت اول ربطی نداره! بخاطره همین خودم 2 فرض کردم!!:30:
.....................
جواب قسمت دوم سوال 16 :
پی اچ محلول سولفوریک اسید 0.001 مولار 2.72 ه !
......................
و ادامه سوال 15(!) :
خب حالا بقیش یه خورده عجیب غریبهههه...!!!
واکنش اول که انجام شد 1 مولار آمونیوم با نیم مولار کربنات واکنش داد---->0.5مولار آمونیوم + 0.5مولار بیکربنات + 0.5 مولار آمونیاک تشکیل شدن!
واکنش دوم بین آمونیوم و بیکراته! یعنی این (با ثابت 3-^10 * 1.3):
nh[SUB]4[/SUB][SUP]+[/SUP] + hco[SUB]3[/SUB][SUP]-[/SUP] === h[SUB]2[/SUB]co[SUB]3[/SUB] + nh[SUB]3[/SUB]
که غلطت تعادلی h2co3 میشه: 4-^10 * 6.4
و غلظت تعادلی hco3 هم میشه: 0.49
پی اچ بافر هم میشه 9.2 .......!!!!!
...................
میدونم دارم چرت میگم کامل، گفتم که بنظر خیلی عجیبه راهم!!!!:4:
راستش من فک کردم پی کا=1.92 که نوشتید، مربوط میشه به قسمت دوم سوال و به قسمت اول ربطی نداره! بخاطره همین خودم 2 فرض کردم!!:30:
.....................
جواب قسمت دوم سوال 16 :
پی اچ محلول سولفوریک اسید 0.001 مولار 2.72 ه !
......................
و ادامه سوال 15(!) :
خب حالا بقیش یه خورده عجیب غریبهههه...!!!
واکنش اول که انجام شد 1 مولار آمونیوم با نیم مولار کربنات واکنش داد---->0.5مولار آمونیوم + 0.5مولار بیکربنات + 0.5 مولار آمونیاک تشکیل شدن!
واکنش دوم بین آمونیوم و بیکراته! یعنی این (با ثابت 3-^10 * 1.3):
nh[SUB]4[/SUB][SUP]+[/SUP] + hco[SUB]3[/SUB][SUP]-[/SUP] === h[SUB]2[/SUB]co[SUB]3[/SUB] + nh[SUB]3[/SUB]
که غلطت تعادلی h2co3 میشه: 4-^10 * 6.4
و غلظت تعادلی hco3 هم میشه: 0.49
پی اچ بافر هم میشه 9.2 .......!!!!!
...................
میدونم دارم چرت میگم کامل، گفتم که بنظر خیلی عجیبه راهم!!!!:4:
آخرین ویرایش توسط مدیر
پاسخ : .> ماراتون شیمی تجزیه! <.
سئوال 16 پس كامل شد!
ميمونه سئوال 15...
ببين، با مقايسه ثابت تعادل واكنش nh[SUB]4[/SUB][SUP]+[/SUP] + hco[SUB]3[/SUB][SUP]-[/SUP] === h[SUB]2[/SUB]co[SUB]3[/SUB] + nh[SUB]3 [/SUB]در جهت رفت و واكنش nh[SUB]4[/SUB][SUP]+[/SUP] + co[SUB]3[/SUB][SUP]2-[/SUP] === hco[SUB]3[/SUB][SUP]-[/SUP] + nh[SUB]3[/SUB] بايد به يه نتايج ديگه اي برسي...
شما توي تعادل دوم، اول در جهت رفت واكنشو كامل فرض كردي و بعدشم از برگشت تعادل به سمت چپ صرفنظر كردي، بجاش رفتي سراغ تعادل اول در جهت رفت! كجاش غلطه؟!
--------
دوستاني كه توي بحث شركت نمي كنين، 11 بدون جوابه كماكان! سئوال خوبيم هست بخدا! يالا ديگه!
از شلاله خانم هم خاهش مي كنم اطلاعات سئوالو تكميل كنن!
pK1? pK2?
و اينكه:58: آيا حد اشباع H2S رو در نظر بگيريم يا نه!
سئوال 16 پس كامل شد!
ميمونه سئوال 15...
ببين، با مقايسه ثابت تعادل واكنش nh[SUB]4[/SUB][SUP]+[/SUP] + hco[SUB]3[/SUB][SUP]-[/SUP] === h[SUB]2[/SUB]co[SUB]3[/SUB] + nh[SUB]3 [/SUB]در جهت رفت و واكنش nh[SUB]4[/SUB][SUP]+[/SUP] + co[SUB]3[/SUB][SUP]2-[/SUP] === hco[SUB]3[/SUB][SUP]-[/SUP] + nh[SUB]3[/SUB] بايد به يه نتايج ديگه اي برسي...
شما توي تعادل دوم، اول در جهت رفت واكنشو كامل فرض كردي و بعدشم از برگشت تعادل به سمت چپ صرفنظر كردي، بجاش رفتي سراغ تعادل اول در جهت رفت! كجاش غلطه؟!
--------
دوستاني كه توي بحث شركت نمي كنين، 11 بدون جوابه كماكان! سئوال خوبيم هست بخدا! يالا ديگه!
سوال 11 :
چند مول HCl را باید به محلولی که از 0.2 مول H2S و 1 لیتر آب تهیه شده، بیافزاییم تا
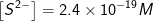 شود ؟ :7:
شود ؟ :7:
چند مول HCl را باید به محلولی که از 0.2 مول H2S و 1 لیتر آب تهیه شده، بیافزاییم تا
pK1? pK2?
و اينكه:58: آيا حد اشباع H2S رو در نظر بگيريم يا نه!
آخرین ویرایش توسط مدیر
- ارسال ها
- 177
- لایک ها
- 112
- امتیاز
- 0
اگه اجازه بدین، سوال 17 تجزیه رو خودم بزارم!
نمیدونم چجوری معادله ها رو بزارم اما حلش اینه:
معادله ی آلفا (معادله ی کسر ترکیب) 2 رو می نویسیم(به صورت تابعی از غلظت یون هیدروژن) بعد آلفا 2 رو به صورت عددی بدست می آوریم(غلظت -S2 تقسیم بر غلظت فرمال اولیه)
معادله رو حل می کنیم
چون خود اسید هیدروژن کمی نسبت به اسید افزوده شده تولید می کنه و چون باز مزدوج غلظت خیلی پایینی رو داره، غلظت یون هیدروژن رو با غلظت فرمال اسید یکی می گیریم (فکر کنم تا 2 یا 3 رقم درست باشه) بعد اون با توجه به حجم ظرف، میزان مول Hcl رو حساب می کنیم
نمیدونم چجوری معادله ها رو بزارم اما حلش اینه:
معادله ی آلفا (معادله ی کسر ترکیب) 2 رو می نویسیم(به صورت تابعی از غلظت یون هیدروژن) بعد آلفا 2 رو به صورت عددی بدست می آوریم(غلظت -S2 تقسیم بر غلظت فرمال اولیه)
معادله رو حل می کنیم
چون خود اسید هیدروژن کمی نسبت به اسید افزوده شده تولید می کنه و چون باز مزدوج غلظت خیلی پایینی رو داره، غلظت یون هیدروژن رو با غلظت فرمال اسید یکی می گیریم (فکر کنم تا 2 یا 3 رقم درست باشه) بعد اون با توجه به حجم ظرف، میزان مول Hcl رو حساب می کنیم
آخرین ویرایش توسط مدیر
پاسخ : .> ماراتون شیمی تجزیه! <.
داده ها وا3 سوال 11: pK[SUB]1[/SUB]=7 و pK[SUB]2[/SUB]=12.88 در نظر بگیرید...
...................
به جناب tesukuyomi : احیانن منظورتون این نیست؟؟!!:

...................
بله :4:....
پس مجدد همون واکنش رو در نظر میگیریم، منتها عکسش!( ثابش هم میشه:0.086 )
پی اچ نهایی میشه: 9.16 تقریبن!

داده ها وا3 سوال 11: pK[SUB]1[/SUB]=7 و pK[SUB]2[/SUB]=12.88 در نظر بگیرید...
...................
به جناب tesukuyomi : احیانن منظورتون این نیست؟؟!!:
...................
ميمونه سئوال 15...
ببين، با مقايسه ثابت تعادل واكنش nh[SUB]4[/SUB][SUP]+[/SUP] + hco[SUB]3[/SUB][SUP]-[/SUP] === h[SUB]2[/SUB]co[SUB]3[/SUB] + nh[SUB]3 [/SUB]در جهت رفت و واكنش nh[SUB]4[/SUB][SUP]+[/SUP] + co[SUB]3[/SUB][SUP]2-[/SUP] === hco[SUB]3[/SUB][SUP]-[/SUP] + nh[SUB]3[/SUB] بايد به يه نتايج ديگه اي برسي...
شما توي تعادل دوم، اول در جهت رفت واكنشو كامل فرض كردي و بعدشم از برگشت تعادل به سمت چپ صرفنظر كردي، بجاش رفتي سراغ تعادل اول در جهت رفت! كجاش غلطه؟!
ببين، با مقايسه ثابت تعادل واكنش nh[SUB]4[/SUB][SUP]+[/SUP] + hco[SUB]3[/SUB][SUP]-[/SUP] === h[SUB]2[/SUB]co[SUB]3[/SUB] + nh[SUB]3 [/SUB]در جهت رفت و واكنش nh[SUB]4[/SUB][SUP]+[/SUP] + co[SUB]3[/SUB][SUP]2-[/SUP] === hco[SUB]3[/SUB][SUP]-[/SUP] + nh[SUB]3[/SUB] بايد به يه نتايج ديگه اي برسي...
شما توي تعادل دوم، اول در جهت رفت واكنشو كامل فرض كردي و بعدشم از برگشت تعادل به سمت چپ صرفنظر كردي، بجاش رفتي سراغ تعادل اول در جهت رفت! كجاش غلطه؟!
پس مجدد همون واکنش رو در نظر میگیریم، منتها عکسش!( ثابش هم میشه:0.086 )
پی اچ نهایی میشه: 9.16 تقریبن!

آخرین ویرایش توسط مدیر
- ارسال ها
- 177
- لایک ها
- 112
- امتیاز
- 0
پاسخ : .> ماراتون شیمی تجزیه! <.

سوال 17:
محلولی آبی داریم،مقداری اضافی روی هیدروکسید در آن می ریزیم
روی در محیط آبی دارای تعدل های زیر است:
Zn(OH)2(s)<==========> Zn(OH)2(aq) pK=5.4
Zn(OH)2(S)<=========>Zn2+ + 2OH- pK=17
Zn2+ + H2O<===========> ZnOH+ + H+ pK=5.7
Zn(OH)2(s) + OH- <============> Zn(OH)3- pK=3.2
Zn(OH)2(s) + 2OH- <=========> Zn(OH)4[2-] pK=2
غلظت هیدروژن را در چه مقداری تنظیم کنیم تا کمتریم میزان ممکن از نمکی روی هیدروکسید حل شود؟(مولکولی را نیز در نظر بگیرید)

سوال 17:
محلولی آبی داریم،مقداری اضافی روی هیدروکسید در آن می ریزیم
روی در محیط آبی دارای تعدل های زیر است:
Zn(OH)2(s)<==========> Zn(OH)2(aq) pK=5.4
Zn(OH)2(S)<=========>Zn2+ + 2OH- pK=17
Zn2+ + H2O<===========> ZnOH+ + H+ pK=5.7
Zn(OH)2(s) + OH- <============> Zn(OH)3- pK=3.2
Zn(OH)2(s) + 2OH- <=========> Zn(OH)4[2-] pK=2
غلظت هیدروژن را در چه مقداری تنظیم کنیم تا کمتریم میزان ممکن از نمکی روی هیدروکسید حل شود؟(مولکولی را نیز در نظر بگیرید)
پاسخ : .> ماراتون شیمی تجزیه! <.
در شرایط معمولی یک گونه شیمیایی با فرمول ساده no[sub]2[/sub] به صورت مخلوطی از دو گونه گازی no[sub]2[/sub] ، n[sub]2[/sub]o[sub]4[/sub] در حال تعادل میباشد .......در 45 درجه سانتی گراد و فشار کل 1 اتمسفر چگالی نمونه ای که فقط دارای این دو گونه است 2.56 گرم بر دسی متر مکعب است . درصد جرمی هریک از گونه ها در یک نمونه چقدر است ؟
در شرایط معمولی یک گونه شیمیایی با فرمول ساده no[sub]2[/sub] به صورت مخلوطی از دو گونه گازی no[sub]2[/sub] ، n[sub]2[/sub]o[sub]4[/sub] در حال تعادل میباشد .......در 45 درجه سانتی گراد و فشار کل 1 اتمسفر چگالی نمونه ای که فقط دارای این دو گونه است 2.56 گرم بر دسی متر مکعب است . درصد جرمی هریک از گونه ها در یک نمونه چقدر است ؟
پاسخ : .> ماراتون شیمی تجزیه! <.
از فرمول P.V=n.R.T
حجم که 1 لیتر هست فشار 1 اتمسفر دما 273+45 کلوین و ثابت گاز هم 0.0821
n رو بدست میاریم که مجموع تعداد مولکول ها هست که میشه حدود 0.0383 مول
حالا جمع مول این دوگاز رو داریم وزن اون رو هم داریم.. از یک 2معادله 2 مجهول مول هرکدوم رو بدست میاریم سپس جرم یکی از گاز ها رو حساب میکنیم تا کسر مولی بدست بیاد. در 100 ضرب میکنیم درصد معلوم میشه
42x+92y=2.56
x+y=0.0383
x=0.021 تعداد مول NO2
y=0.0173 تعداد مول N2O4
یک راه دیگه هم داره که تقریبا همینه ولی یکم تغییر شکل یافتشه!
چگالی=(فشار در جرم مولی) تقسیم بر (دما در ثابت گازها)
که همین فرمول هست فقط جاگذاری شده
از فرمول P.V=n.R.T
حجم که 1 لیتر هست فشار 1 اتمسفر دما 273+45 کلوین و ثابت گاز هم 0.0821
n رو بدست میاریم که مجموع تعداد مولکول ها هست که میشه حدود 0.0383 مول
حالا جمع مول این دوگاز رو داریم وزن اون رو هم داریم.. از یک 2معادله 2 مجهول مول هرکدوم رو بدست میاریم سپس جرم یکی از گاز ها رو حساب میکنیم تا کسر مولی بدست بیاد. در 100 ضرب میکنیم درصد معلوم میشه
42x+92y=2.56
x+y=0.0383
x=0.021 تعداد مول NO2
y=0.0173 تعداد مول N2O4
یک راه دیگه هم داره که تقریبا همینه ولی یکم تغییر شکل یافتشه!
چگالی=(فشار در جرم مولی) تقسیم بر (دما در ثابت گازها)
که همین فرمول هست فقط جاگذاری شده
- ارسال ها
- 2,708
- لایک ها
- 3,152
- امتیاز
- 0
پاسخ : .> ماراتون شیمی تجزیه! <.
بچه ها ببخشید نمیدونم شماره ی سوال چنده. هر کی میدونه بهم بگه ویرایش کنم و شماره بذارم.
برای احیای بخش شیمی میخوام اینجا سوال بذارم. ببخشید اگه سوالش اسونه انشالله به مرور زمان سوالای سخت تر میذارم. الان سوال دم دست ندارم!
ا) ثابت یونیزاسیون آب را حساب کنید غلطت یون h مثبت در اب خالص برابر 10[SUP]7- [/SUP]
است.
ب) ثابت کنید اسید HA برابر با K[SUB]a[/SUB] است. ثابت تعادل واکنش های زیر را محاسبه کنید.
A+H<----- >HA
A بار منفی و H مثبت و همه در حالت aq
A+H2O <-----> HA+OH[SUP]
A و OH بار منفی همه در حالت aq بجز اب در حالت مایع
[/SUP]
بچه ها ببخشید نمیدونم شماره ی سوال چنده. هر کی میدونه بهم بگه ویرایش کنم و شماره بذارم.
برای احیای بخش شیمی میخوام اینجا سوال بذارم. ببخشید اگه سوالش اسونه انشالله به مرور زمان سوالای سخت تر میذارم. الان سوال دم دست ندارم!
ا) ثابت یونیزاسیون آب را حساب کنید غلطت یون h مثبت در اب خالص برابر 10[SUP]7- [/SUP]
است.
ب) ثابت کنید اسید HA برابر با K[SUB]a[/SUB] است. ثابت تعادل واکنش های زیر را محاسبه کنید.
A+H<----- >HA
A بار منفی و H مثبت و همه در حالت aq
A+H2O <-----> HA+OH[SUP]
A و OH بار منفی همه در حالت aq بجز اب در حالت مایع
[/SUP]
پاسخ : .> ماراتون شیمی تجزیه! <.
I)
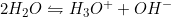

II) البته فکر کنم منظورتون این بوده که ثابت اسید HA برابره با
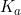 من با این فرض به سوال جواب دادم:
من با این فرض به سوال جواب دادم:
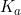

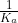
 البته این واکنش ها با اونایی که شما نوشتین فرقی ندارن و فقط یون هیدروژن به صورت یون هیدرونیوم آبپوشیده شده.
البته این واکنش ها با اونایی که شما نوشتین فرقی ندارن و فقط یون هیدروژن به صورت یون هیدرونیوم آبپوشیده شده.
III)


)

)

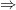 اگه اشکالی داشت لطفا بگین.:67:
اگه اشکالی داشت لطفا بگین.:67:
بچه ها ببخشید نمیدونم شماره ی سوال چنده. هر کی میدونه بهم بگه ویرایش کنم و شماره بذارم.
برای احیای بخش شیمی میخوام اینجا سوال بذارم. ببخشید اگه سوالش اسونه انشالله به مرور زمان سوالای سخت تر میذارم. الان سوال دم دست ندارم!
ا) ثابت یونیزاسیون آب را حساب کنید غلطت یون h مثبت در اب خالص برابر 10[SUP]7- [/SUP]
است.
ب) ثابت کنید اسید HA برابر با K[SUB]a[/SUB] است. ثابت تعادل واکنش های زیر را محاسبه کنید.
A+H<----- >HA
A بار منفی و H مثبت و همه در حالت aq
A+H2O <-----> HA+OH[SUP]
A و OH بار منفی همه در حالت aq بجز اب در حالت مایع
[/SUP]
برای احیای بخش شیمی میخوام اینجا سوال بذارم. ببخشید اگه سوالش اسونه انشالله به مرور زمان سوالای سخت تر میذارم. الان سوال دم دست ندارم!
ا) ثابت یونیزاسیون آب را حساب کنید غلطت یون h مثبت در اب خالص برابر 10[SUP]7- [/SUP]
است.
ب) ثابت کنید اسید HA برابر با K[SUB]a[/SUB] است. ثابت تعادل واکنش های زیر را محاسبه کنید.
A+H<----- >HA
A بار منفی و H مثبت و همه در حالت aq
A+H2O <-----> HA+OH[SUP]
A و OH بار منفی همه در حالت aq بجز اب در حالت مایع
[/SUP]
II) البته فکر کنم منظورتون این بوده که ثابت اسید HA برابره با
III)
آخرین ویرایش توسط مدیر
